今年的诺贝尔化学奖,意味着我们从此不需要科学家了? 复杂系统研究的胜利
2024年诺贝尔化学奖的揭晓为科学界带来了新的亮点。美国科学家大卫·贝克因在蛋白质结构设计领域的开创性工作荣获一半奖金,而另一半奖金则授予了英国科学家德米斯·哈萨比斯与美国科学家约翰·江珀,表彰他们在蛋白质结构预测方面的杰出贡献。这两大成就虽新,却共同指向一个历史悠久的挑战:如何仅凭蛋白质的一维氨基酸序列预测其复杂的三维结构。

蛋白质作为生命体内的核心化学成分,负责从构造到生化功能的众多任务。尽管科学家早已能测定氨基酸序列,但蛋白质需从线性链转变为特定的三维形态才能发挥功能,其功能差异主要源自结构的不同。这一过程类似乐高积木,相同的组件能搭建出多样作品,价值取决于最终结构。
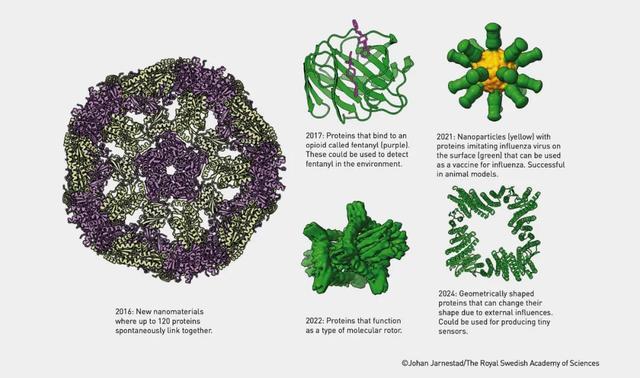
蛋白质的三维结构形成看似神奇,实则基于氨基酸的物理化学属性,如亲水性、疏水性及电荷间的相互作用,促使蛋白质自发折叠成能量最低状态,如同乐高模型能快速自我重组。然而,尽管原理直观,基于氨基酸序列准确预测蛋白质复杂三维结构仍极具挑战,特别是考虑到蛋白质由成千上万氨基酸组成,包含多层次的结构。
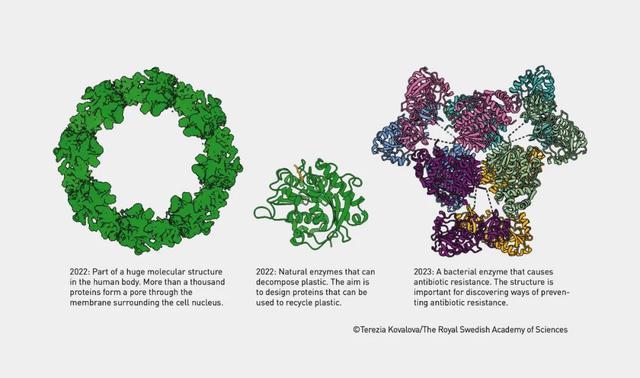
X射线晶体衍射技术的运用,如在揭示DNA双螺旋结构时那样,为结构解析提供了途径,但仍受限于蛋白质结晶的难度和成本。中国科学家颜宁在此领域成绩斐然,但该方法无法解决所有问题。

大卫·贝克自1993年起,在蛋白质结构预测软件罗塞塔(Rosetta)的开发上取得突破,不仅在国际竞赛中持续领先,还开放了软件供公众使用,展现出难得的开源精神。随后,DeepMind团队凭借AlphaFold系列软件,特别是在AlphaFold2上的显著成就,大幅推进了预测精度,几乎达到实验级准确度,极大促进了新药研发等领域的发展。
AlphaFold3的推出更是将预测精度提升至前所未有的水平,覆盖了生命分子的广泛范围,展示了人工智能在复杂系统研究中的潜力。然而,尽管人工智能在处理大量数据和复杂计算方面表现出色,人类科学家在总结普遍规律和处理生物学中非线性、灵活变化现象的能力依然不可或缺,尤其是在面对如蛋白质磷酸化和无序蛋白等复杂现象时。
今年的诺贝尔奖,尤其是化学奖,突显了复杂系统研究的重要性,无论是microRNA的基因调控、神经网络的模拟,还是蛋白质结构的探索,都体现了科学向理解及模拟复杂系统转变的趋势,预示着科研范式的变革正在发生。这些奖项不仅是人工智能的胜利,更是对复杂系统深刻理解的胜利。
本文来自互联网用户投稿,该文观点仅代表作者本人,不代表本站立场。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如若转载,请注明出处:http://www.rxxp.cn/wsHL/156351.html
如若内容造成侵权/违法违规/事实不符,请联系一条长河网进行投诉反馈邮箱:809451989@qq.com,一经查实,立即删除!